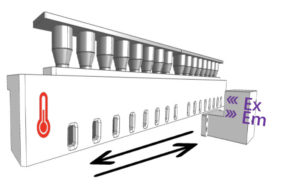
Мультифункциональный анализатор стабильности белков PSA-16
Дифференциальная сканирующая флуориметрия (DSF) — это быстрый, надежный, высококачественный метод анализа стабильности белков, их температур плавления и термодинамических параметров на основе флуоресценции триптофана. DSF является отличным инструментом для скрининга буферов и детергентов. В целом, флуоресценция триптофана сильно зависит от третичной структуры белка и определяется его локальной микросредой, включая расположение и окружение аминокислотных остатков. При воздействии высоких температур или химических детергентов белки теряют свою нативную структуру, что приводит к изменениям спектра флуоресценции триптофана. DSF отслеживает эти изменения с высоким временным разрешением и может выявить даже несколько конформационных переходов. Важно отметить, что дополнительного окрашивания образов не требуется, буфер может быть любым. Поэтому DSF высоко эффективен при разработке антител, изучении мембранных белков, контроле качества белка, скрининге буферов, анализе разворачивания белка и скрининге связывания низкомолекулярных соединений.
Прибор не требует предварительного нагрева, очистки и обслуживания. Система интегрирована с управляющим компьютером для сбора и анализа данных. Пробирки для образцов из высокочистого кварца с высоким УФ-пропусканием позволяют работать с образцами низкой концентрации и не требуют предварительной обработки. Конструкция пробирок в формате стрипов по 8 полосок обеспечивает гибкость при загрузке образцов. Пробирки имеют герметичную конструкцию, предотвращающую испарение образца во время эксперимента.
Принцип метода nanoDSF:
- При возбуждении на 280 нм белок испускает флуоресценцию, обусловленную эмиссией триптофана.
- Спектр флуоресценции триптофана тесно связан с его микроокружением.
- В свернутом состоянии триптофан находится в гидрофобном ядре белка. После разворачивания белка триптофан оказывается в растворителе.
- В процессе разворачивания пик эмиссии триптофана смещается с 330 нм на 350 нм.
- Измеряемые параметры: Tm, Ton, Cm, ΔG.
- Изменение соотношения между значениями флуоресценции при 350 нм и 330 нм может быть использовано для мониторинга процесса разворачивания белка.
- Возможна работа в агрессивных средах, например можно проводить измерения мембранных белков в детергентной среде.
- Скрининг буферов
- Скрининг детергентов
- Контроль качества белков
- Контроль условий хранения
- Модификация белков
- Анализ термического сдвига
- Идентификация серотипа AAVS
- Сравнение производственных партий
- Изотермическая стабильность
- Рефолдинг белков
| Измерение | Тм, Тон, См,ΔG, Изотермическая стабильность, Термическая стабильность |
| Пропускная способность | 16 образцов/прогон |
| Время тестирования | 10~60 мин |
| Объем пробы | ≤20 мкл |
| Концентрация | 0,05 мг/мл~300 мг/мл |
| Сбор данных | 20 точек данных на образец за 1 минуту (быстрое индивидуальное сканирование, со сбором данных каждые 3 секунды). |
| Точность | Значение Tm CV<1% Tm value CV<1% |
| Диапазон температур | 15 — 110℃ |
| Точность температуры | ±0,2℃ |
| Скорость нагрева | 0,1 — 15℃/минута, регулируемая |
| Длина волны | 330±5 нм и 350±5 нм |
В целом, флуоресценция триптофана сильно зависит от их 3D-структуры белка и, следовательно, от локального окружения аминокислотных остатков. При использовании химических детергентов или высокой температуры белки могут разворачиваться, что приводит к изменениям спектра автофлуоресценции триптофана. NanoDSF отслеживает эти изменения с высоким временным разрешением и может выявить даже несколько конформационных переходов. Поэтому NanoDSF весьма эффективен при разработке антител, изучении мембранных белков, контроле качества белка, скрининге буфера, анализе разворачивания белка и скрининге связывания низкомолекулярных соединений.
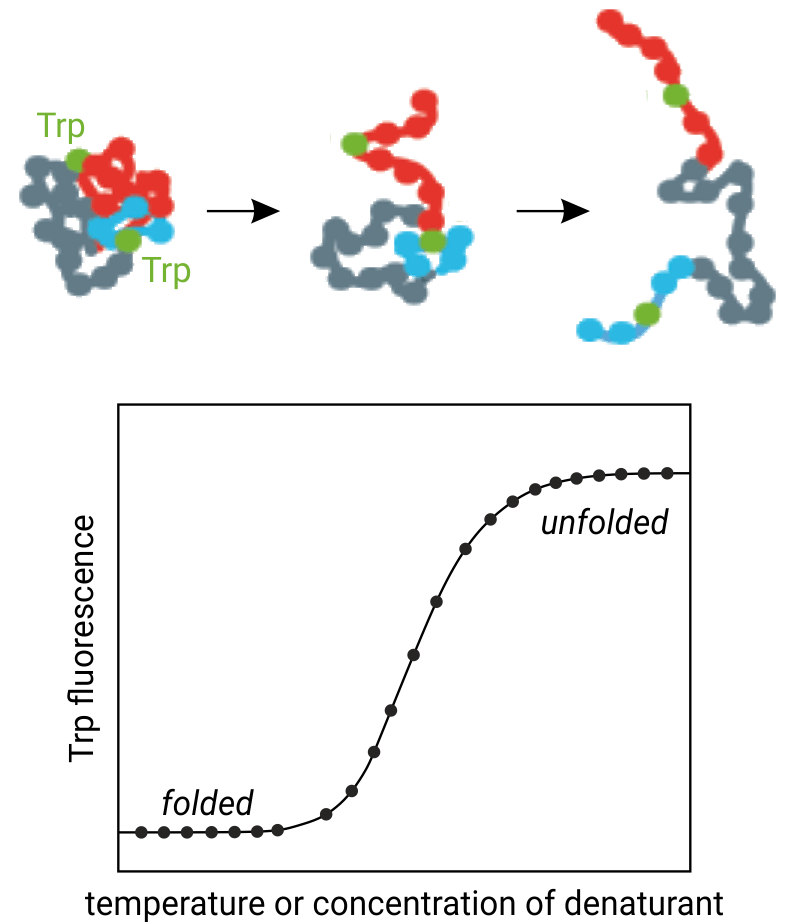
Рисунок 1. Принцип, лежащий в основе термической денатурации белка: повышение температуры вызывает денатурацию третичной структуры белка и, таким образом, остатки триптофана, подвергаются воздействию растворителя. NanoDSF отслеживает параллельные изменения флуоресценции триптофана на длинах волн 330 и 350 нм.
Конформационная стабильность белка описывается его средней температурой денатурации Tm (°C), которая является точкой, где разворачивается половина белка. Метод nanoDSF основан на детекции флуоресценции триптофана (и в меньшей степени тирозина), которая очень чувствительна и изменяется при термическом разворачивании.
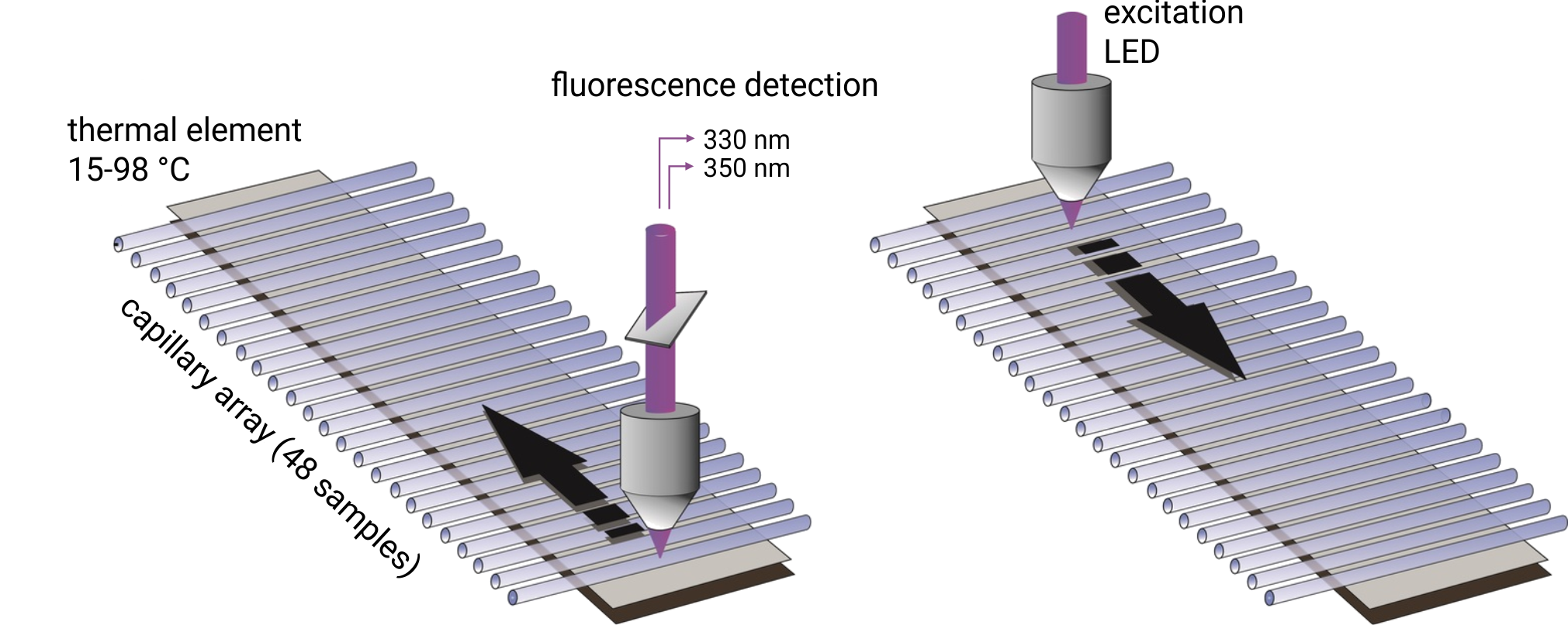
Производятся измерения флуоресценции на длинах волн 330/350 нм. Температуры плавления регистрируются путем мониторинга изменений флуоресценции триптофана. Важно отметить, что дополнительного окрашивания образов не требуется, буфер может быть любым.